Hóa trị là gì? Quy tắc hóa trị của nguyên tố hóa học là khái niệm hình thành nhưng liên kết hóa học quen thuộc. Khi biết hóa trị của một nguyên tố ta sẽ lập được công thức hóa học của hợp chất mà chúng ta cần tìm. Kiến thức hóa học cơ bản hôm nay sẽ giúp các bạn học sinh nắm về quy tắc hóa trị cụ thể nhất với những ví dụ dễ hiểu nhất!
1. Hóa trị là gì?
– Hóa trị của nguyên tố hóa học là con số biểu thị khả năng liên kết của nguyên tử (hay nhóm nguyên tử) của nguyên tố này với nguyên tử của nguyên tố khác. Giá trị này được xác định bằng bằng số liên kết hóa học mà một nguyên tử của nguyên tố đó tạo nên trong phân tử.
– Hóa trị của một nguyên tố được xác định theo hóa trị của H chọn làm đơn vị (H hóa trị I) và hóa trị của O là hai đơn vị (O hóa trị II).
– Hóa trị của một nhóm nguyên tố cũng tương tự như trên (nhóm nguyên tử được coi như một nguyên tố bất kỳ)
– Bảng hóa trị của các nguyên tố hóa học và Bảng hóa trị của một số nhóm nguyên tử được chúng tôi tổng hợp hóa trị của các nguyên tố và nhóm nguyên tử thường gặp nhất.
– Để ghi nhớ hóa trị của các nguyên tố hóa học và nhóm nguyên tử thì học sinh cần có phương pháp học tập và rèn luyện hiệu quả. Các bạn có thể tham khảo cách nhớ hóa trị của các nguyên tố hóa học nhé!
2. Quy tắc hóa trị của nguyên tố hóa học
Trong công thức hóa học, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
 |
| Hóa trị - Quy tắc hóa trị của các nguyên tố hóa học |
Cho CTHH AxBy, nguyên tố A có hóa trị a, nguyên tố B có hóa trị B. Ta có:
x.a = y.b
Ứng dụng của quy tắc hóa trị
Theo quy tắc hóa trị: x.a = y.b, ta có thể vận dụng như sau:
– Tính hóa trị của một nguyên tố ⇒ Nếu biết x,y và a thì tính được b và ngược lại.
– Lập CTHH của hợp chất ⇒ Nếu biết a và b thì tìm được tỉ lệ: x/y = b/a. Từ đó ta lập được CTHH của hợp chất cần tìm.
3. Ví dụ
3.1. Lập công thức hóa học của hợp chất theo hóa trị
- Sắt (II) oxit được tạo nên từ nguyên tố sắt (Fe) có hóa trị III và oxi (O) có hóa trị II. Lập công thức hóa học của oxit sắt trên.
Bài giải:
Gọi CTHH của oxit sắt là FexOy, theo quy tắc hóa trị ta có: x.III = y.II
⇒ Tỉ lệ x/y = 2/3
Vậy CTHH của oxit sắt cần tìm là: Fe2O3.
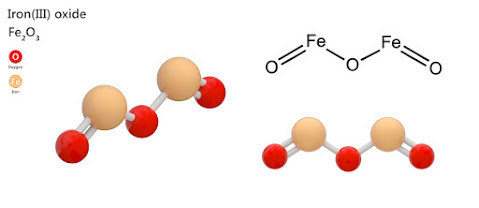 |
| Công thức cấu tạo của iron (III) oxide |
3.2. Cách xác định hóa trị của nguyên tố hóa học
- Hóa trị của nguyên tố được xác định theo hóa trị của Hidro (1 đơn vị) và hóa trị của oxi (2 đơn vị). Ví dụ:
+ Cl có hóa trị I trong phân tử HCl
+ O có hóa trị II trong phân tử H2O
+ N có hóa trị III trong phân tử NH3
- Có những nguyên tố chỉ có một hóa trị và cũng có những nguyên tố có hai hay nhiều hóa trị. Ví dụ:
+ H có 1 hóa trị là I.
+ C có hóa trị II và IV.
+ S có hóa trị II, IV, VI
- Lập công thức hóa học của hợp chất tạo bởi lưu huỳnh VI và Oxi
– Công thức tổng quát dạng: SxOy
– Theo quy tắc hóa trị: x.VI = y.II
– Ta lập tỉ lệ: x/y= II/VI =1/3
– Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất, vì vậy lấy: x = 1 và y = 3.
⇒ Công thức hóa học của hợp chất: SO3
Lời kết
Hy vọng bài viết Quy tắc hóa trị của nguyên tố hóa học đã giúp các em hiểu quy tắc, cách tính hóa trị của nguyên tố, nhóm nguyên tử hóa học. Ngoài ra, các em cần nắm thêm bảng hóa trị của các nguyên tố hóa học để vận dụng làm bài tập hiểu quả hơn. Chúc các em học tốt nhé!






















0 Nhận xét